베트남 약품 관리국( 보건부 )에 따르면, 오늘 9월 27일 F. Hoffmann La Roche Ltd. 대표 사무소에서 공식 발송 번호 RA/02/09/2023을 발행하여 Avastin 약물과 관련된 조사에 대한 최신 정보를 보고했습니다.
이전에 이 부서는 파키스탄 당국으로부터 스위스 제약 회사인 로슈가 유통한 암 치료제의 사용을 일시적으로 금지한다는 정보를 받았는데, 이는 12명의 환자가 해당 약물을 주사받은 후 실명했기 때문입니다.

베트남에서는 아바스틴이 4개의 유효한 유통 등록증을 취득했습니다.
베트남 의약품 관리국에 따르면, 베트남에서는 특정 암 치료에 사용되는 약물인 아바스틴이 4개의 유효한 등록증을 보유하고 있습니다. 이 약물은 특정 적응증과 경고가 포함된 등록증을 발급받습니다.
특히, 이 약물은 전이성 대장암, 진행성, 전이성 또는 재발성 비소세포 폐암, 진행성 및/또는 전이성 신세포 암종, 신경교종, 악성 신경교종(4기), 상피성 난소암, 나팔관암, 원발성 복막암 환자에게 적응증이 있습니다.
일반적인 경고 외에도 FDA 승인 패키지 삽입물에는 "유리체내 사용 금지"에 대한 경고가 포함되어 있습니다.
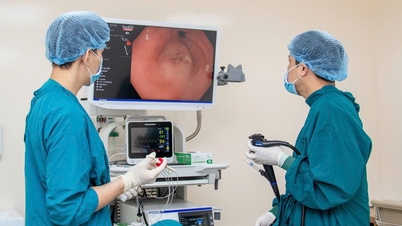
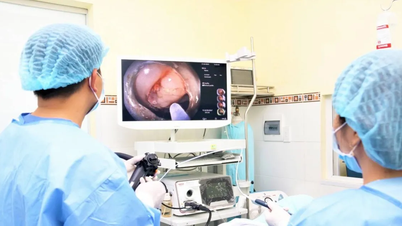
이 약물은 시각 장애를 유발할 수 있습니다. 암 환자에게 정맥용 바이알을 사용하여 아바스틴을 유리체강 내 투여한 후 심각한 안구 이상반응이 개별 사례 및 군집으로 보고되었습니다. 이는 다음과 같은 반응의 가능성으로 인해 허용되지 않는 투여 경로입니다. 안구 내 감염, 무균성 안구 내염, 포도막염 및 유리체염과 같은 안구 내염, 망막 밴딩, 망막 색소 상피 열상, 녹내장, 유리체 또는 망막 출혈과 같은 안구 내 출혈, 결막 출혈. 이러한 이상반응 중 일부는 영구 실명을 포함한 다양한 정도의 시력 상실을 초래했습니다.
베트남 약물 관리국 관계자는 베트남에서 아바스틴을 사용한 후 시력을 잃은 환자와 관련된 부작용을 반영하는 보고를 아직 접수하지 못했다고 밝혔습니다.
F. 호프만 라 로슈(F. Hoffmann La Roche Ltd.) 대표 사무소 보고서에 따르면, 파키스탄에서 아바스틴 관련 조사에 대한 최신 정보가 공개되었습니다. 불법 공급업체인 제니어스 파마슈티컬 서비스(Genius Pharmaceutical Service)에서 공급한 주사제를 사용한 환자 약 12명이 시력을 잃었습니다. 해당 약물은 "아바스틴 1.25mg/0.05ml 주사제"라는 라벨이 붙어 있어 로슈 제품이라는 잘못된 인식을 불러일으켰습니다.
로슈의 아바스틴은 안과용으로 승인되지 않았습니다. Genius Pharmaceutical Service는 비위생적이고 승인되지 않은 조건에서 1.25mg/0.5ml 용량을 공급, 희석 및 재포장했습니다.
파키스탄 당국은 오염의 가능한 원인을 파악하기 위해 조사하고 있는데, 여기에는 부적절한 살균, 오염된 바이알, 살균되지 않은 주사기, 약물 분배 시의 표준 운영 절차 위반 등이 포함됩니다.
[광고_2]
소스 링크


![[사진] 팜민친 총리, 지방자치단체와 온라인 정부 회의 주재](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/10/5/264793cfb4404c63a701d235ff43e1bd)

![[사진] 팜민친 총리, 제14차 전국당대회 기념 성과 달성 위한 최고 모방 캠페인 전개](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/10/5/8869ec5cdbc740f58fbf2ae73f065076)
















































![[영상] 페트로베트남 50주년 기념식 요약](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/10/4/abe133bdb8114793a16d4fe3e5bd0f12)

![[영상] 람 사무총장, 페트로베트남에 8가지 황금 단어 수여: "선구자적, 탁월함, 지속 가능성, 글로벌"](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/7/23/c2fdb48863e846cfa9fb8e6ea9cf44e7)


































댓글 (0)